复发性肝细胞癌(HCC)作为高发恶性肿瘤,热物理消融是局部肿瘤治疗的重要手段,且能通过促进肿瘤抗原的释放,激活全身性抗肿瘤免疫。然而,传统局部消融方法诱导的免疫响应不足以诱导足够强烈的免疫保护。多模态肿瘤治疗(MTT)是一种新型局部消融技术,通过多物理模态融合技术,实现肿瘤细胞精准破碎,原位大量释放的肿瘤抗原与危险信号分子(DAMPs)可作为“原位疫苗”,肿瘤完全消融同时系统性调节全身免疫环境。
av解说 徐学敏、刘苹团队联合医学院苏冰团队和复旦大学附属肿瘤医院李文涛团队,在《Theranostics》(IF=13.3)发表重磅研究,首次揭示:多模态肿瘤治疗通过释放大量危险信号分子(DAMPs)激活树突状细胞,促进CX3CR1+GPR56+肿瘤反应性T细胞扩增,并降低调节性T细胞(Tregs)比例,从而显著延长肝癌患者无进展生存期(PFS),为复发性肝癌介入免疫治疗提供全新机制与靶点。

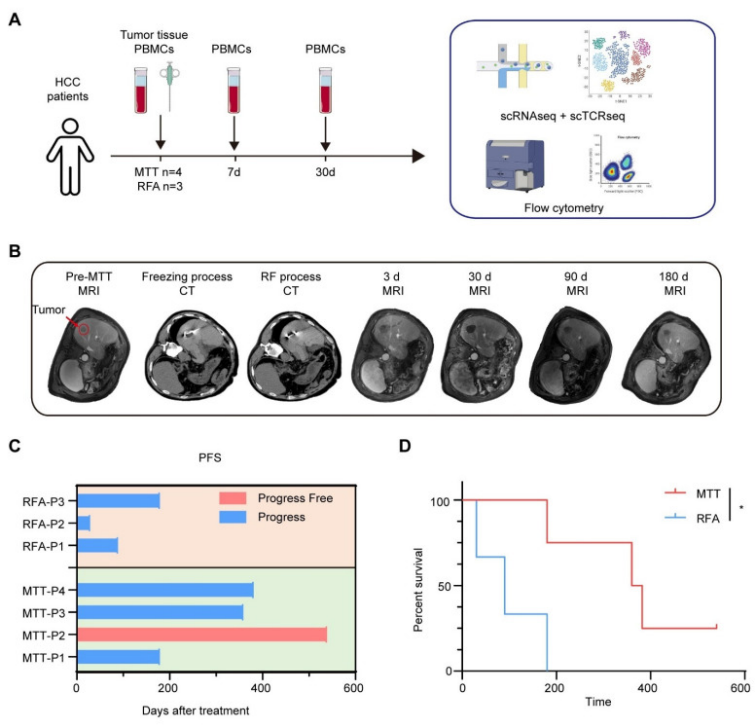
图1 研究方案及患者生存结局
为深入探究多模态肿瘤治疗延长患者PFS的免疫学机制,通过对患者术前肿瘤组织、外周血,以及术后7天、30天外周血连续采样,结合单细胞转录组测序、单细胞TCR测序、流式细胞术等技术,全面刻画治疗前后的免疫景观动态变化;同时构建小鼠肝癌皮下肿瘤模型,验证关键免疫细胞亚群的功能与调控通路。研究发现,两组患者治疗前免疫景观无明显差异,而在治疗后,多模态肿瘤治疗组患者较RFA组患者树突状细胞成熟、NK细胞毒性分子表达、B细胞体液免疫应答上调,并诱导了CX3CR1+GPR56+ T细胞扩增,同时Tregs比例显著下调。结合动物模型研究证明,CX3CR1+GPR56+ T细胞高表达颗粒酶B、穿孔素、等效应细胞因子,并具有更强的向瘤内迁移的能力。治疗后7天CX3CR1评分与患者PFS呈正相关,提示多模态肿瘤治疗诱导的CX3CR1+GPR56+ 效应T细胞比例增加,是HCC患者良好临床预后的生物标志物。
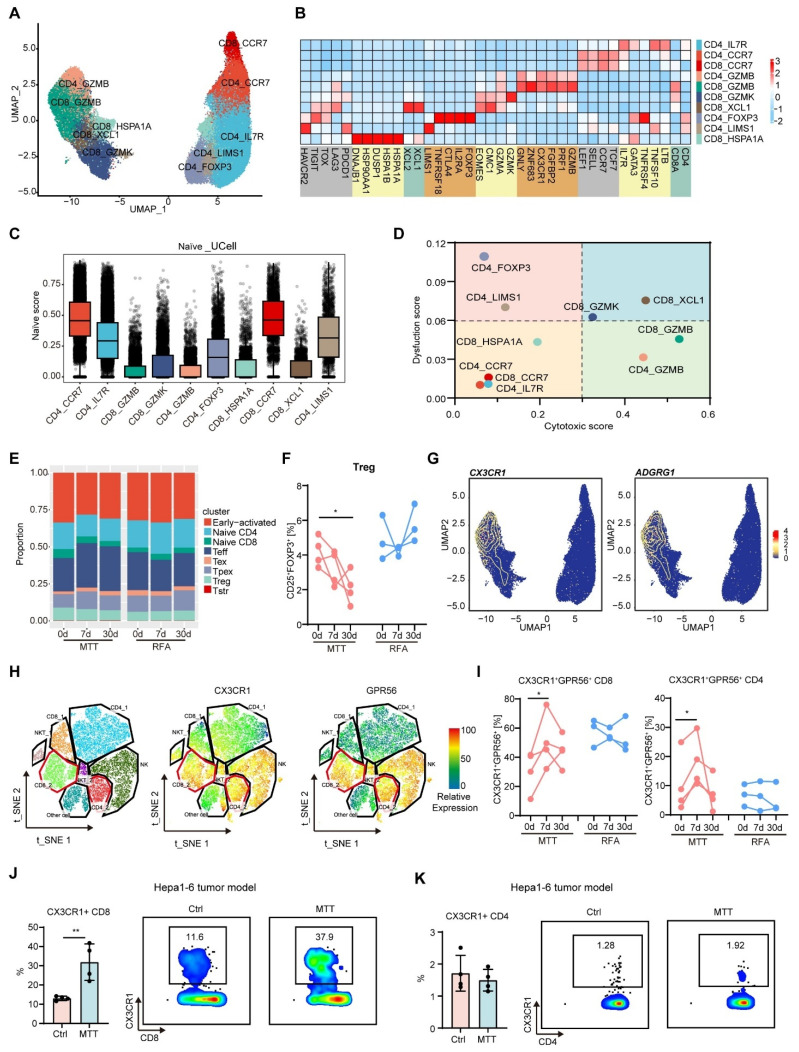
图2 接受多模态肿瘤治疗患者外周血中效应T细胞比例增加,Tregs比例下调
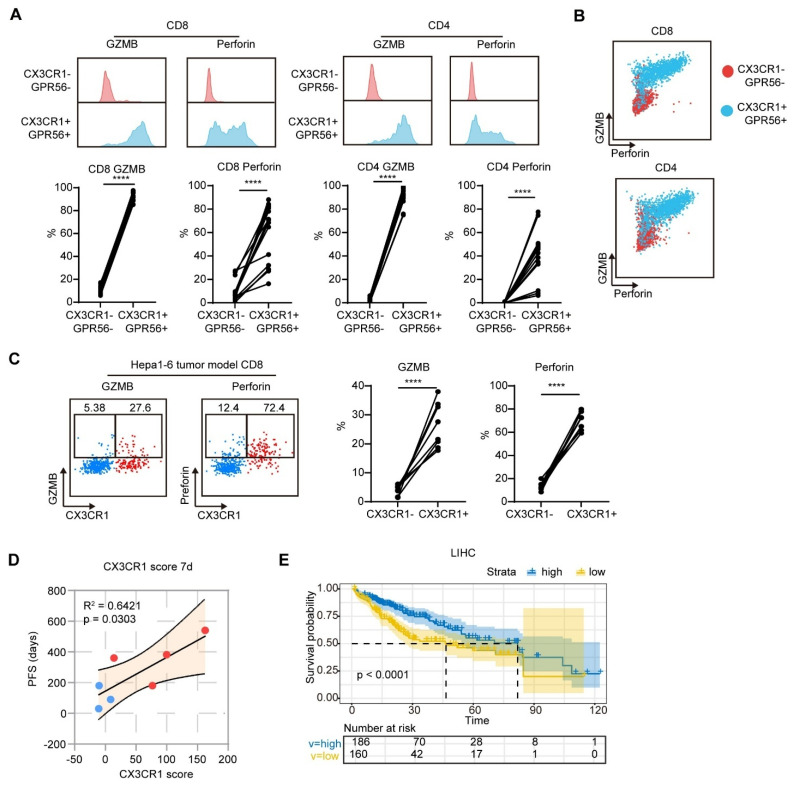
图3 CX3CR1+ T细胞毒性分子表达升高
研究进一步通过单细胞TCR测序联合生物信息学分析,对其肿瘤反应性进行了系统验证。结果显示,外周血CX3CR1+GPR56+CD8+ T细胞与肿瘤内富集的肿瘤反应性T细胞(Ttr-like)共享高度同源的TCR序列,其TCR克隆型在肿瘤组织中存在显著扩增,证实该群细胞具备精准识别肿瘤抗原的核心特征。体外自体抗原共培养实验显示,CX3CR1+GPR56+ T细胞在接触肿瘤细胞后可大量分泌IFN-γ,证明其具备肿瘤特异性识别与应答能力。与此同时,研究通过TCR谱系追踪证实,多模态肿瘤治疗可显著驱动CX3CR1+GPR56+肿瘤反应性T细胞发生克隆性扩增,而这一现象在RFA组中并未出现,进一步说明CX3CR1+GPR56+ T细胞可能是介导多模态肿瘤治疗抗肿瘤免疫效应的关键功能性亚群。
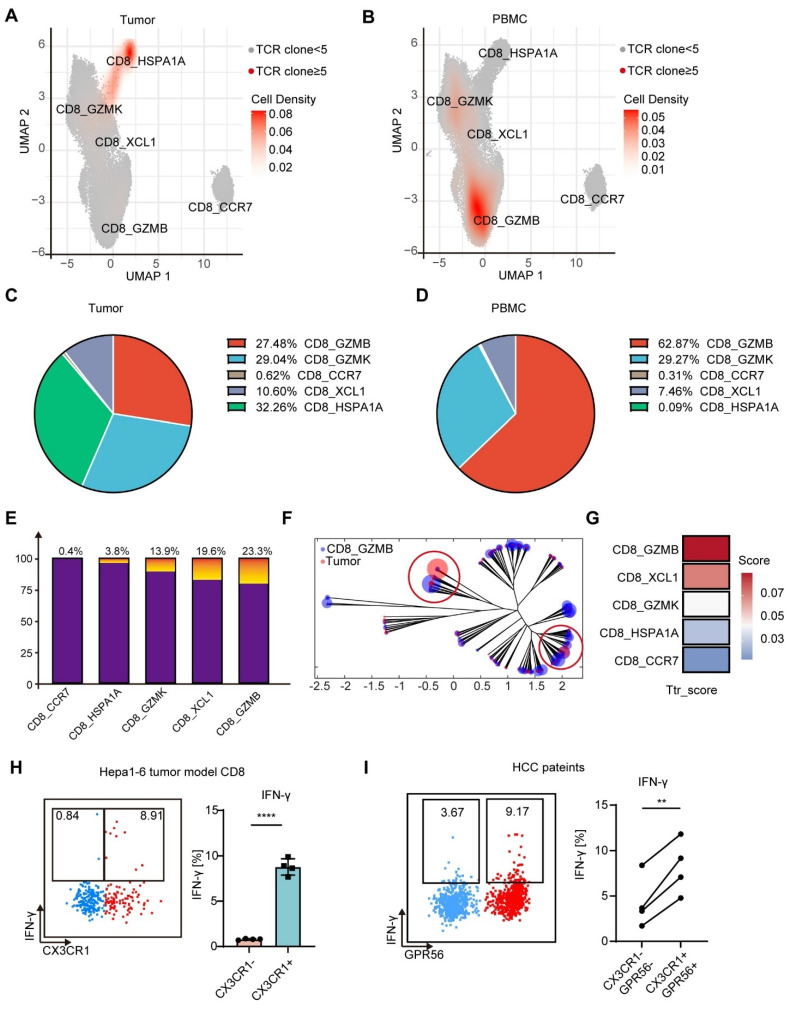
图4 血液中效应CD8+ T细胞在肿瘤反应性样T细胞中富集
在此基础上,研究进一步解析了多模态肿瘤治疗驱动免疫重塑的分子机制。研究发现,多模态肿瘤治疗可诱导肿瘤细胞发生免疫原性死亡,大量释放热休克蛋白(HSP70)、胞外DNA等损伤相关分子模式(DAMPs),这些信号分子能够有效激活树突状细胞的Toll样受体(TLR)信号通路与胞质DNA感知通路,显著提升其抗原呈递能力。与RFA治疗相比,多模态肿瘤治疗后树突状细胞与CX3CR1+GPR56+效应T细胞之间的MHC-I-TCR相互作用显著增强,直接驱动肿瘤反应性T细胞的克隆扩增;同时,多模态肿瘤治疗可下调树突状细胞与Tregs之间的LGALS9-CD45信号轴,削弱Tregs的分化与免疫抑制功能。借助小鼠双侧肝癌模型,研究还证实局部多模态肿瘤治疗治疗能够触发系统性抗肿瘤免疫,重塑远端未治疗病灶的免疫微环境,增加效应T细胞与记忆性T细胞浸润,减少髓系来源抑制细胞(MDSCs)积累,从而诱导远隔效应。
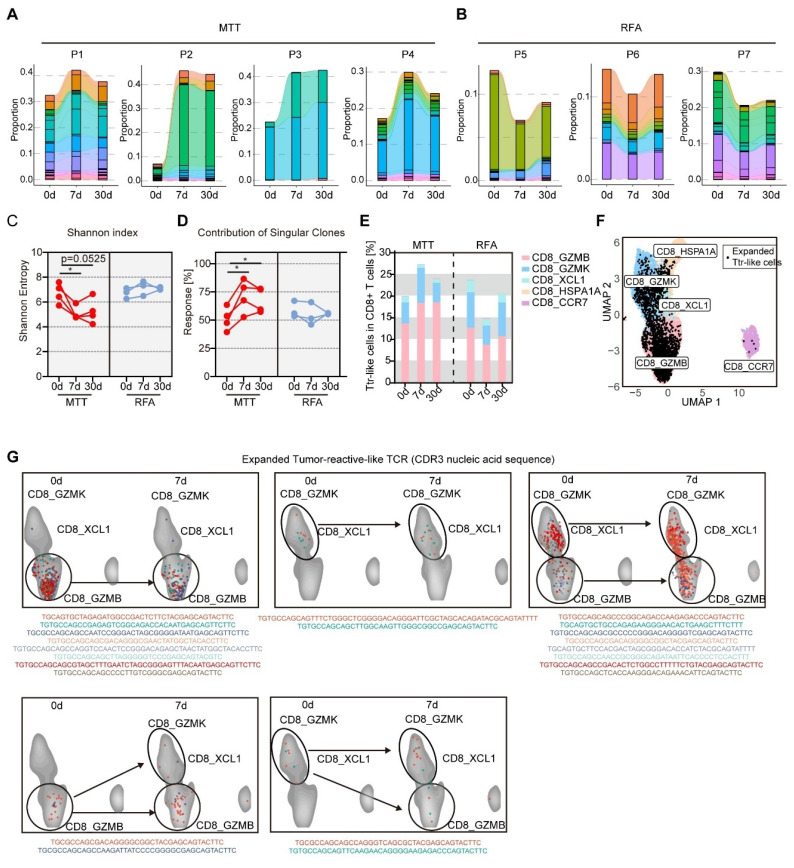
图5 多模态肿瘤治疗促进CX3CR1+GPR56+肿瘤反应性样T细胞克隆扩增
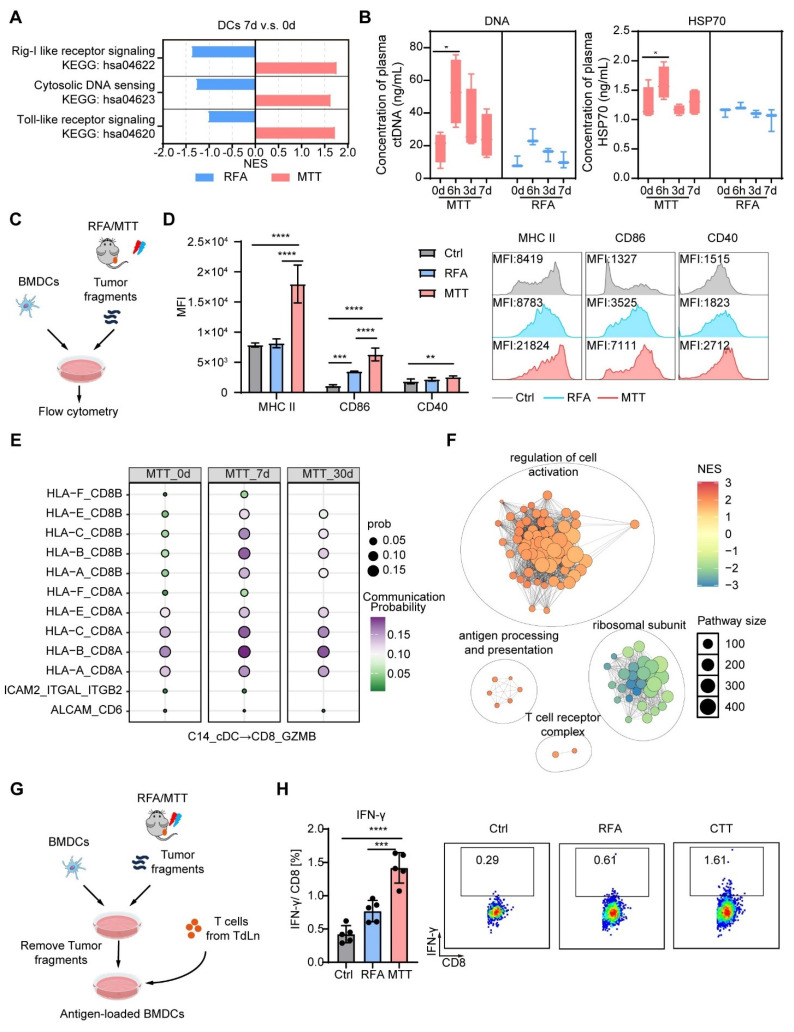
图6 多模态肿瘤治疗通过促进树突状细胞成熟诱导肿瘤反应性样T细胞扩增
该研究首次在肝癌患者中阐明了多模态肿瘤治疗诱导持久抗肿瘤免疫的核心机制,并发现CX3CR1+GPR56+ T细胞可作为无创外周血标志物,用于预测多模态肿瘤治疗获益人群。多模态肿瘤治疗作为平台型微创介入技术,可与免疫检查点抑制剂、细胞治疗等联合应用,打破实体肿瘤免疫治疗瓶颈,为肝细胞癌乃至更多实体瘤的治疗提供了从局部消融到全身免疫调控的全新策略,具有重要的临床转化前景。
原文信息:Wang S, Wang Y, Zhang Y, et al. Multimodal tumor thermal therapy enhances antitumor immunity by expanding tumor-reactive CX3CR1+GPR56+ T cells in hepatocellular carcinoma. Theranostics, 2026;16(12):4959-4978. DOI: 10.7150/thno.103682
